|
編輯組報導
美國食品藥物管制局(FDA)經過漫長的審查,終于在2014年4月公佈,不主張用子宮絞碎器,施行子宮切除或子宮肌瘤切摘除手術。 美國婦科腹腔鏡醫學會,美國婦癌醫學會,和美國婦產科醫學會咸認為子宮絞碎器,對低風險的病人,仍勝於傳統腹部手術,有存在的需要。醫學會也都認為,仔細挑選病人,改善手術前子宮癌的篩檢才是首要。 腹腔鏡子宮絞碎手術,常用於切除子宮或子宮肌瘤,美國每年行這類手術約有10萬次,至為普遍。由於手術後組織檢查,發現原本認為良性的子宮肌瘤卻隱藏了子宮肉瘤等惡性組織(約1/350),癌細胞因絞碎手術而擴散,因此,近年來爭端不少。 絞碎手術是經由腹腔鏡,用子宮絞碎機,將子宮或子宮肌瘤切成片狀,組織便容易從陰道或腹腔鏡的小手術口取出。 這次子宮絞碎機爭議的背景,以及發展,簡述如下: 2013年10月,貝斯以色列醫療中心41歲麻醉科Amy Reed醫師,因為子宮肌瘤在波士頓伯明罕婦女醫院,接受了絞碎手術進行子宮切除。手術後1星期病理報告發現有子宮肉瘤,而且癌症已擴散到腹腔,惡症屬於第四期。 Reed醫師因此接受了腫瘤減積手術和腹腔內溫熱化療,以及六個週期的合併化療(gemcitabine 和 docetaxel)。隨後核磁共振和電腦斷層沒有顯示癌症。 2015年2月她回賓州大學醫院工作,又發現她的上左腿麻痺,骨盆腔核磁共振掃描發現她的左腎後方有一個腫瘤,侵犯了她的脊椎和第二腰椎脊椎神經。2月20日,由神經外科醫師執行手術切除腫瘤以及進行椎板切除和腰椎融合手術。腫瘤化驗結果是癌變,細胞與她的子宮肉瘤一樣。Reed醫師現正接受大約數週的放療。 Reed醫師的先生,伯明罕婦女醫院心臟胸腔外科Hooman Noorchashm醫師,同時也是哈佛醫學院外科講師表示,Reed醫師是在美國哈佛大學醫學中心伯明罕婦女醫院接受治療,手術前做了許多檢查,包含MRI,2次超音波和子宮內膜切片檢查,並經由婦癌科和放射科醫師診斷,才決定由腹腔鏡做子宮切除,手術時間兩個小時,當天回家。Reed醫師在手術兩天後便到處走,一切都是在計劃中。手術一週後,才知道有癌症,而且癌症已經擴散。 由於該項手術有未知癌組織的風險,Noorchashm醫師夫婦乃全力的推動禁止子宮絞碎手術,並要求修改醫療儀器的安全法規。除了FDA於2014年不贊成子宮絞碎手術並增加了更強硬的黑框警語外。健康醫療產業也快速回應,嬌生公司主動從市場上撤回絞碎手術儀器。美國HCA聯營醫院也禁止使用絞碎手術。美東健康保險公司,Highmark更停止支付婦科絞碎手術的健保費。 由于化療對已有轉移的子宮肉瘤效果並不好,減積手術治療也甚勉強。這對醫師夫婦,因此同時也著手善用他們的資源,共同來協助她們對付敵人—癌症。標靶治療,mTOR抑制劑,和T細胞免疫治療,雖然仍大部分在臨床測試中,將會是Reed醫師往後在放療後,可能會用上的抗癌藥物。 Reed醫師並計劃,針對抑制這種少見的特殊癌細胞從事研究。她和她的先生Noorchashm醫師,對免疫學都有更深的研究,也曾有共同的著作。 中英名詞對照 貝斯以色列醫療中心Beth Israel Deaconess Medical Center腹腔內溫熱化療hyperthermic intraperitoneal chemotherapy 椎板切除laminectomy 腰椎融合術lumbar fusion 子宮絞碎機power morcellator 子宮肉瘤uterine sarcoma 美國腹腔鏡醫師學會American Association of Gynecologic Laparoscopists 婦科腫瘤學會The Society of Gynecologic Oncology 美國婦產科學會The American College of Obstetricians and Gynecologists 參考資料
編輯組
mTOR( ridaforolimus)美國臨床腫瘤期刊6月報導,加拿大多倫多市Princess Margaret癌症中心,Amit. M. Oza醫師團隊研究顯示,抑制細胞增生傳遞的mTOR抑制劑,ridaforolimus,能改善晚期子宮內膜癌無惡化存活,唯副作用太大。根據研究指出,患有晚期子宮內膜癌病人中,5年無惡化存活只有12%。靜脈注射ridaforolimus讓1/3的婦女在臨床上受惠。標靶藥確實能有效治療原發晚期子宮內膜癌,藥物毒性和卻是治療過程中的一大挑戰,需要積極的監控。研究從全球36個的醫療據點,總病人130,在開放式研究中比較,口服mTOR抑制劑,ridaforolimus和黃體素或化療。相較於比較組,Ridaforolimus組平均無惡化存活的時間顯著較長,分別是3.6個月和1.9個月(p=0.008);無惡化存活率也高於比較組,在16週時分別為18%和18%;24週,是38%和15%。針對病人達到疾病穩定狀態,ridaforolimus組(35% )顯著高於比較組(17%),但ridaforolimus組無人達到治療目標反應,比較組則有4%病人達到。總存活率沒有顯著差異,ridaforolimus組是10.0個月;比較組是9.6個月。與比較組(6%)相較,ridaforolimus 組(33%)有更多病人因副作用,停止參與治療研究;同時,嚴重副作用,有57%,比較組,34%。Ridaforolimus組最常見發生的治療後副作用程度是3至4級,分別有高血糖,貧血,口腔炎或口腔黏膜發炎,腹瀉以及虛弱。治療晚期子宮內膜癌增加標靶藥,Bevacizumab 美國東區醫學中心,醫學科學主任Maurie Markman認為,以臨床醫療的角度而論,2015年美國臨床腫瘤學會年會中最重要研究發表,是義大利研究團隊的第二階段隨機研究:白金藥(carboplatin)和紫杉醇(paclitaxel)合併治療再加上標靶藥(bevacizumab),治療復發或原發的晚期子宮內膜癌。 病人因此在加此標靶藥後(108人),會提升了反應率,分別是72.7%和54.3%,以及無惡化存活,分別是13.0和8.7個月 (P = .036)。該研究數據與卵巢癌的第三階段研究結果一致。 子宮內膜癌治療的標準carboplatin/paclitaxel合併化療,加上抗血管生成藥bevacizumab,有利預後。唯需要小心挑選病人,以及治療方案會造成高血壓和其它血管的合併症。 名詞中英對照 子宮內膜癌endometrial carcinoma 參考資料1. Oza AM, et al. Ridaforolimus shows some promise in advanced endometrial carcinoma. J Clin Oncol 2015. 2. Markman M. Adding bevacizumab for advanced endometrial cancer. 編輯組報導
美國密西根州底特律聯邦法院7月10日宣判,底特律腫瘤科Farid Fata醫師,為了謀利,故意誤診病人,給病人過量和不必要的化療藥,其中還包含沒有癌症的病人,達553人,行為囂張,匪夷所思,重判入獄45年。 由於Fata醫師的腫瘤科診所員工,向聯邦調查員告發相關的不法行徑,2013年8月他因而遭到逮捕。他最離譜的罪行,莫過於告訴健康的病人罹患了多發性骨髓癌和其他的癌症,讓這些無辜病人,不但接受了不必要且長期的化療之外,還要承受瀕臨死亡的心理煎熬。 根據聯邦檢察官調查,該醫師透過誤診和欺騙病人,讓病人接受不必要,超量的化學治療療程,不法謀利至少1千7百萬美元。範圍含蓋該醫師所擁有的腫瘤科診所,和分布在底特律郊區的7個相關處所;藥局,診斷檢測中心,放射治療中心,和一個令人睥睨的假慈善機構。受害病人總共有553人。 Fata醫師於逮捕一年後,承認犯下:13項醫療詐欺,兩項洗錢,一項向臨終照護與家庭醫療機構收取回扣等罪行。 法院作證道出: (1)一位病人家屬Laura Stedtefelt表示,該醫師對她患有肺癌的父親過度治療,造成父親死亡。她認為Fata醫師謀害了父親且臨終前讓他身體飽受折磨。 (2)病人Maggie Dorsey指出,Fata醫師故意誤診,聲稱她罹患多發性骨髓瘤,給予化療藥,bortezomib治療。她含淚描述嚴重的骨質疏鬆和神經病變副作用,令 她有段時間她無法站立,大部分的夜晚因太過疼痛而無法入睡。 (3)另一個病人表示,他從未得過多發性骨髓癌,Fata醫師卻用zoledronic acid治療他,讓他因副作用而掉光了所有的牙齒。 Fata以超過醫療準則的藥物劑量來治療癌症的病人;對於疾病緩解的病人,仍然定期的開立終身持續劑量的化療藥處方;病人臨終前,仍持續給予癌症4期的化療劑量。同時,還經常告訴病人其病情已有超過70%甚至更多的緩解機會,給予病人虛假的希望。 美國司法部要求法院將Fata醫師判刑監禁175年,眾多加重刑期的原因之一是,他的行為,無法原諒,讓民眾對專業醫療喪失信心。美國底特律法官認為Fata醫師犯下了非常重大恐怖的連續犯罪行為。Fata醫師也承認錯用專業,自己毀了自己,貪念關閉了他曾有的惻隱之心。 名詞中英對照 多發性骨髓瘤multiple myeloma 參考資料 Physician who gave unneeded chemo gets 45 years in prison. Medscape. Jul 10, 2015. 編輯組報導
加拿大安大略省WellMedica醫院家庭醫學科Eric Grief醫師,透過Medscap醫療網部落格建立醫師自信計劃,針對病例狀況提出詢問,並建立網路問卷,與醫療人員討論醫病溝通議題。 病例 最近有位62歲已婚女士的轉診病人,有四個成年子女和幾個孫子。因轉移性乳癌,癌細胞已轉移至骨頭,前額,肝臟等。她的健康狀況正在下滑,家屬希望能幫助這位女士處理焦慮和沮喪的情緒。 當這位女士以平常的步履走進我的診間時幾乎就要跌倒,她不願抱怨因癌症身體所承受的疼痛。但,當我問及為何來,以及對疾病的感覺時,她再也無法控制自己的情緒。她表示很不喜歡失去獨立能力,也不希望因為疾病惡化需要照顧而成為家人的負擔。她的丈夫在一旁勸她要堅強和持續運動。這位女士仍然嘗試堅忍,但我已讓她情緒放鬆,並準備告訴我她的痛苦與沮喪。但她仍不願意向家人,家庭醫師和癌症主治醫師吐露她的感受。 她責備自己一開始就不應該與醫師有這類的討論,她自2006年開始治療癌症至今還未準備好能夠與人討論患病感受。 問題 當病人有轉移癌症時,誰有責任最先與病人討論情緒感受?應該一開始就將這個責任留給病人或是病人家屬嗎?或是應該由家庭醫師或癌症主治醫師負起這項責任呢? 精神科jherschler醫師表示,所有提供治療的單位應準備好探究病人情緒的困境。採用開放式的詢問方式,如:你好嗎?你還可以嗎?這類發問可以開啟一些混亂情緒的討論,與同坐病人身旁也能提供支持的力量和親切的感覺。因為精神狀況而轉診的情況若真的發生,應是超出個人診間所能處理的狀況。 醫學院學生douglas表示,當病人聽到自己罹患癌症的時刻,所有事情都會因此停止。如果無法與人討論,他們會變得孤立,也難怪會感到沮喪,就像被判了死刑一般。 問卷結果 有27%的人認為,應由病人先主動討論,應尊重病人的選擇權利。27%人認為,應該是家屬先與病人討論情緒感受,接下來是親屬然後是親近的朋友。27%的人認為癌症主治醫師應先與病人討論。沒有人認為家庭醫師或主要醫療單位應先與病人討論。 參考資料 Eric Grief, MD, Family Medicine. When patients have metastatic cancer, who initiates the discussion about feelings? MD-Rap (Medical doctor real-time assertiveness program). Jan 31, 2015 編輯組報導
美國知名醫療網Medscape 2月依據臨床腫瘤醫學報導,抗腫瘤藥,Eribulin,第三階段臨床研究數據指出,患有晚期軟組織肉瘤病人,接受eribulin ( Halaven, Eisain),治療後,與接受化療藥,dacarbazine的病人相較,顯著增加病人總存活率。 2015年美國約有12,000診斷罹患軟組織肉瘤,死亡約有4700。早期診斷出軟組織肉瘤可透過手術治癒;晚期或轉移性病人的預後不佳,平均存活不超過1年。 Eribulin已於2010年為美國乳癌核准用藥,並獲得美國食品藥物局核准為治療軟組織肉瘤的孤兒藥。今年底該藥廠將以第三階段研究數據,申請治療肉瘤的上市核准。 治療肉瘤的新數據來自於309個隨機開放性研究,涵蓋452位患有局部晚期或復發或轉移的脂肪囊狀性細胞肉瘤或平滑肌肉瘤,且已接受了兩種標準治療後仍惡化的病人(病人必須接受過小紅莓類化療藥,且失敗後至少有再接受一項其他治療)。 治療方法以21天為一治療週期。eribulin組,於週期第一天和第八天給予eribulin mesylate靜脈注射1.4毫克/平方米。dacarbazine組病人,則在週期第一天給予靜脈注射850毫克/平方公尺到1200毫克/平方米。 結果顯示,eribulin組的總存活率顯著較長。顯示eribulin具有治療軟組織肉瘤的潛力。最常見的副作用,是嗜中性粒細胞減少症,疲勞,噁心,掉髮和便秘。 名詞中英對照 脂肪囊狀性細胞肉瘤adipocytic sarcoma 平滑肌肉瘤leiomyosarcoma 參考資料 1. Eribulin improves survival in advanced sarcoma. Medscape. Feb 26, 2015. 2. Schöffski P, Maki RG, Italiano A, et al. Randomized, open-label, multicenter, phase III study of eribulin versus dacarbazine in patients (pts) with leiomyosarcoma (LMS) and adipocytic sarcoma (ADI). J Clin Oncol. 2015;(suppl; abstr LBA10502). 3. Schöffski P, Ray-Coquard IL, Cioffi A, et al. Activity of eribulin mesylate in patients with soft-tissue sarcoma: a phase 2 study in four independent histological subtypes. Lancet Oncol. 2011;12(11):1045-1052. 編輯組報導
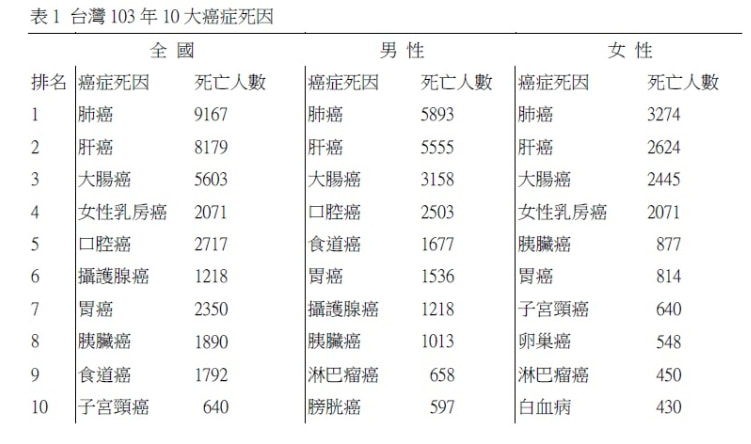
美國外科學院期刊2月報導美國路易斯安那州大學健康中心Quyen Chu醫師研究指出,接受乳房切除手術治療的局部晚期乳癌病人,1/3病人在手術後未依治療準則接受放療。 根據美國國家癌症網(NCCN)和美國臨床腫瘤學會的準則,局部晚期乳癌,細胞已擴散至4個以上窩腋淋巴結(N2/N3)的病人,是復發和死亡的高風險族群。手術後放療可改善治療結果。 國家癌症資料庫中採樣(1998至2011)診斷為N2/N3乳癌病人的病歷,以評估對治療準則的遵守程度。 癌症委員會研究期間共有2百72萬名病例,確認56,990位符合。約只有65%的病人以乳房切除手術治療和術後放療。35%的病人未接受術後放療,原因仍然是個謎。 研究指出,手術後放療對於局部晚期乳癌病人有利益,可降低局部病灶復發20%至27%,同時可增加總存活8%至9%。 名詞中英對照 美國國家綜合癌症網National Comprehensive Cancer Network,NCCN 美國臨床腫瘤學會American Society of Clinical Oncology,ASCO 放療radiation therapy, RT 參考資料 Chu Q, et al. 'Puzzle': 35% of High-Risk Mastectomy Patients Get No RT.J Am Coll Surg. Published online January 14, 2015. 編輯組報導 衛生福利部公布103年國人10大死因統計報告指出,十大死因以慢性病為主。惡性腫瘤自71年起已連續33年高居國人死因之首,且死亡率遠超過第二位心臟疾病之死亡率2倍之多,分別是28.3%與12%。103年平均11分24秒就有一人死於癌症。 103年癌症總死亡人數為46,094,占總死亡人數28.3%。以肺癌和肝癌續居前10大癌症死因前兩位。依序為氣管、支氣管和肺癌;肝和肝內膽管癌;結腸、直腸和肛門癌;女性乳房癌;口腔癌;前列腺癌;胃癌;胰臟癌;食道癌;子宮頸及部位未明示子宮癌。順位與去年相同;與10年前,93年相較,順位上升者有口腔癌、前列腺癌與胰臟癌,順位下降者有胃癌及子宮頸癌。尤以胰臟癌上升幅度最大,子宮頸癌下降幅度最大(表1)。 癌症死亡性別差異 前三大癌症死因,兩性均為肺癌、肝癌和結腸直腸癌。男性死亡人數高於女性,差距最大者為食道癌與口腔癌,男性死亡率分別為女性死亡率之14.3倍與11.9倍,且該兩項癌症不在女性10大癌症死因之列;其他癌症,男性約為女性之1.2~2.5倍。與93年標準化死亡率相較,男性以食道癌的上升15.5%最為明顯,女性則為胰臟癌之24.8%。男性以胃癌以30.9%降幅最大,女性則是子宮頸癌,下降52.3%;結腸直腸癌、口腔癌和食道癌,男性呈上升,而女性則下降。 103年國人因癌症死亡者,平均年齡為68.1歲,較93年增長2.2歲。其中男性持平,女性增長3歲。 參考資料
103年國人10大死因統計.衛生福利部統計處.Jun, 17, 2015. 編輯組報導
美國耶魯大學,負責Dana-Farber癌症中心的免疫腫瘤科中心和黑色素瘤治療,F. Stephen Hodi醫師認為,PD-L1將成為預測腫瘤的生物標誌。 研究發現,免疫防禦,原本可撲殺癌細胞,卻因分子阻擾,而失去了防禦的功能。扮演這個角色,是一種稱為計劃細胞死亡蛋白,PD-1。 PD-1屬於CD28家族成員之一,該類蛋白家族中分兩大類,一類具活化免疫細胞功能,另一類則是傳遞抑制功能。PD-1就是屬於抑制T細胞具阻斷功能的蛋白質,PD-L1/L2是其對應的配體,PD-1與PD-L1/L2互相影響運作能防止自身免疫力攻擊組織,卻讓癌細胞藉此躲避掉免疫T細胞的攻擊。 抗體藥,MPDL3280A,為PD-L1阻斷劑,其功能可解除PD-L1對T細胞的抑制,回復T細胞攻擊和摧毀癌細胞的反應力。有研究顯示,這種破解PD-L1檢查站的結果,明顯地縮減腎臟,黑色素瘤,和肺腫瘤體積的能力,相較於其他的免疫治療藥物,表現更為出色。美國耶魯大學醫學院暨Dana-Farber癌症研究所研究指出,對於一開始使用免疫治療藥後免疫力反擊癌細胞,而後被抑制而停止反應的病人,治療效果最好。 自然醫學雜誌去年11月號報導,當病人的免疫細胞環繞著有表現PD-L1抑制蛋白,顯示原有的免疫反應被PD-L1阻斷了,這個時候PD-L1抗體所能發揮的效果最佳。癌細胞未有免疫反應的病人,腫瘤萎縮最少,表示癌細胞和組織周圍的PD-L1也不多。 研究從接受MPDL3280A治療的175位,晚期非小細胞癌,黑色素瘤,腎臟癌和其他癌症病人中,採集腫瘤組織樣本確認。平均治療結果,18%的病人有完全或部份腫瘤萎縮,隨著不同型態的癌症產生出不同程度的比率。總體治療表現,有良好的耐受度,副作用較少。 研究方法是利用一種抗體著色法,能夠標記出PD-L1存在,在病人治療前切除的腫瘤樣本上,揭示出PD-L1不只存在於癌細胞,也存在於腫瘤浸潤免疫細胞內。這表示T細胞和其他免疫細胞已進入腫瘤內部且企圖把腫瘤摧毀。 研究發現,病人的癌細胞和免疫細胞有越高PD-L1,對抗體藥物反應越大。觀察病人在治療期間取得的腫瘤樣本中PD-L1的表現情況,發現已經萎縮的腫瘤當細胞死亡時,顯示癌細胞和浸潤免疫細胞中PD-L1增加。 結論,若要MPDL3280A抗體更有效率,病人必須出現過PD-L1反擊的免疫反應。才可創造瞄準鎖住PD-L1的抗體,去除阻斷免疫反應和允許免疫細胞攻擊腫瘤。 另一研究主持人西班牙塞維利亞市Virgen Del Roccio大學醫院Luis Paz-Ares醫師指出,帶有PDL-1蛋白高程度表達的肺癌病人,也獲得最佳利益,平均總存活率是17.2到19.4個月,是該類型病人有史以來最佳的治療結果。相較於接受第二線紫杉醇,docetaxel治療的病人,平均存活是8至10.4個月。 雖然帶有PDL-1低度表達的病人的藥物反應和存活率相對較低,但部份病人有過反應,因此這個生物標記可用於可能有反應病人的正向預測值,但是無法作為無反應病人的逆向預測值,因此,PDL-I生物標記還未能在臨床使用。 名詞中英對照 計畫性細胞死亡-1 programmed cell death 1, PD-1 計畫性細胞死亡-1配體programmed cell death ligand, PD-1 突圍檢查站checkpoint blocker 參考資料 Hodi FS, Herbst R, et al. Study finds potential predictive biomarker for response to PD-L1 checkpoint blocker. Sam Ogden, Dana-Farber. November 26, 2014. 編輯組報導
美國臨床腫瘤學會2015年會,研究評論人,美國康乃狄克州耶魯癌症中心腫瘤科主任Roy Herbst醫師聲明,臨床治療,因免疫治療藥,nivolumab(必治妥藥廠)而改變。 在CheckMate 057第三階段研究顯示,對於已治療過的鱗狀非小細胞癌病人,Nivolumab,與紫杉醇,docetaxel,化療藥相較,總存活有顯著改善,藥物毒性也明顯較低。是目前最新的標準治療。 非鱗狀類型是兩大類型非小細胞肺癌中,人數最多的類型,約占所有肺癌病人的60%,鱗狀類型占25%。其餘的是小細胞肺癌。 CheckMate 057研究,涵蓋接受鉑金藥雙重化療仍惡化的晚期非鱗狀非小細胞肺癌病人共582人。結果顯示,與docetaxel相較,使用nivolumab治療平均總存活率增加3個月,分別是12.2和9.4個月 (P = .00155)。 美國腫瘤學會專家暨賓州大學Abramson癌症中心腫瘤科Lynn Schuschter醫師評論表示。免疫治療的副作用較特殊:都是與免疫力相關的副作用,與傳統化療產生的副作用相較,較不明顯。因相關副作用而停止治療的病例只有5%;化療docetaxel則有15%。 佛羅里達州坦帕市Moffitt癌症中心胸腔腫瘤助理教授Ben Creelan醫師評論,免疫治療翻轉了肺癌治療。成果是飛躍前進,遠超越了標靶治療。研究結果認為,非小細胞肺癌病人, 20%將可看到腫瘤縮小, 20%病情穩定,因此有40%的病人將可受惠。 免疫治療反應可長期持續,而標靶治療最大的缺點是,經常在6個月內腫瘤產生抗力。自2010年我們曾經用nivolumab或類似的藥物治療肺癌,同時看到病人病情在5年後持續緩解。這些治療反應的續航力非常驚人。參與早期臨床研究的病人,只接受nivolumab,2年的治療,即使日後不再接受藥物,病情也仍持續緩解。 紫杉醇類化療藥, Docetaxel,自從1999年核准後便成為肺癌的第二線標準治療藥。 Nivuolumab的兩次臨床研究,包括鱗狀類與非鱗狀類非小細胞肺癌,各自進行第三階段研究。Nivolumab耐受度優於化療。Docetaxel會引起掉髮,指甲問題,腹瀉,神經病變,白血球下降和疲勞。比較下nivolumab副作用較少。一般治療期間病人可正常生活並可重回職場,同時看起來與一般人無異。 名詞中英對照 非小細胞肺癌nonsmall cell lung cancer ,NSCLC 參考資料 Paz-Ares L, et al. Nivolumab in lung cancer shows 'unprecedented' survival. American Society of Clinical Oncology (ASCO) 2015 Annual Meeting: Abstract LBA109. May 31, 2015. 編輯組報導
新英格蘭醫學期刊報導今年2月歐洲腫瘤學會2014年,CLEOPATRA研究指出,合併抑制腫瘤細胞HER2過度表現的單株抗體,pertuzumab和trastuzumab,加上常用化療藥,紫杉醇,docetaxel,治療轉移性HER2陽性乳癌病人,創造出空前未有的存活率,平均提升近16個月。 原本pertuzumab,便有15.7個月的存活利益。再與trastuzumab及docetaxel三種化療藥合併治療比兩種合併,trastuzumab和docetaxel,平均總存活顯著更佳,分別是56.5和40.8個月(P < .001)。 2011年的研究指出,pertuzumab顯著增加疾病無惡化存活。2012年的中期分析顯示,總存活率顯著改善,且具有臨床意義(P = .0008)。在參與研究病人至少385人死亡後,做最後分析,平均追踪50個月報告指出,兩藥,pertuzumab與rastuzumab合併治療的病人總存活率有顯著改善。 Pertuzumab和trastuzumab皆是人類抗HER2單株抗體標靶藥,合併使用比單獨使用更有效,因為兩藥合併更能全面阻斷癌細胞訊號傳遞。 CLEOPATRA研究,自2008至2010年,從808名未接受HER2陽性轉移性乳癌病人參與。 所有病人:第一週期第二天接受靜脈注射,紫杉醇藥,docetaxel 75 毫克/平方公尺(mg/m²),剩下週期,則在週期第一天注射;第一週期第二天,依體重每一公斤注射8 毫克的trastuzumab,剩下的週期則在第一天依體重每公斤注射6毫克。 另外,所有病人隨機分配至接受pertuzumab組,第一週期第一天注射pertuzumab 840毫克和剩下周期第一天注射420毫克。 治療週期則需觀察所有組別病人直到疾病惡化或出現難以控制的毒性反應為止。不允許減低劑量。 Pertuzumab組死亡人數比安慰劑組少,分別是168(41.8%)與221(54.4%)人(P < .001)。疾病無惡化平均存活,pertuzumab組比安慰劑組多6.3個月,兩組病人主要死亡原因是疾病惡化。 Pertuzumab和trastuzumab加上docetaxel合併治療的安全性與知名的長期雙標靶藥物的安全性一致,副作用機率與初期的分析一致。大部分的副作用在1至2級,都在使用docetaxel時發生。研究過程中持續進行長期的心臟安全檢測, pertuzumab組發生左心室功能失調的機率些微較安慰組低。 研究主持人美國華盛頓哥倫比亞特區MedStar Washington中心醫院頓華盛頓研究所主任Sandra M. Swain醫師於2014年歐洲腫瘤醫學會會議,首次發表結果指出,大家都認為,Pertuzumab合併trastuzumab,作為HER2陽性轉移乳癌的第一線治療,56.5個月平均總存活率是空前的最佳治療結果。另一個來自西班牙巴塞隆納Vall d'Hebron腫瘤研究所乳癌科主任Javier Cortés醫師的研究結果與該研究一致,表示應考慮將這種合併治療作為HER2陽性轉移性乳癌的標準治療。 但是,過去10年癌症治療的費用已經成為一個逐漸受到關注的問題,每當發現一個新的治療,隨之而來的是醫療費用的增加。Trastuzumab費用每個月大約4500美元,更新的pertuzumab費用更高約30%,每月花費6000美元。一個完整療程, pertuzumab與 trastuzumab合併治療將花費10萬9千5百萬美元,且依治療的時間和紫杉醇,taxane(docetaxel),的選擇也會影響治療的花費。 名詞中英對照 歐洲腫瘤醫學會European Society for Medical Oncology,ESMO 第二型人類表皮生長因子接受體Human Epidermal Growth Factor Receptor 2,HER2 參考資料 Swain S M, et al. HER2- positive metastatic breast cancer: new standard of care.N Engl J Med. 2015;372:724-734. |
Copyright © 2018 財團法人中華民國婦癌基金會 All Rights Reserved
會 址:10487臺北市復興北路 178 號 4 樓之 6
聯絡地址:11217臺北市北投區石牌路二段201號中正樓7樓