|
李新揚 博士
台北榮總婦產科生殖內分泌科主治醫生 中華民國生育醫學會秘書長 前言 科學的進步早已讓人類克服許多限制,包括二度空間的穿越:地球上任意兩點都可以在48小時內到達;三度空間的突破:人類漫遊外太空及登陸月球。然而對於時間,第四個象限的限制,仍是一籌莫展,人類自己無法隨意回到過去及未來,也無法凍結時間。 隨著人工生殖技術的進步,我們已能成功冷凍著床前的胚胎、精子及卵子,讓它們在零下150度更低的液態氮環境中,降低甚至暫停細胞代謝,如此可以停留上百年的時間,需要時才行解凍,繼續生命的進展。卵子的冷凍比著床前胚胎及精子的冷凍困難許多,主要是因為卵子細胞較大且水分較多,在冷凍過程中不易脫水,而且成熟卵子的紡綞體也容易受到冷凍傷害。 在自然界也發現有此現象,例如北極蛙可以在零下8℃ 存活兩週以上,最主要是靠在低溫時產生大量的葡萄糖及甘油,此兩種物質是冷凍保護劑,可以避免細胞內形成冰晶。卵子的冷凍方式最早是採用慢速冷凍法,雖然解凍後的成功懷孕率有逐漸改善,但是仍不夠理想。最近幾年改用快速冷凍法,卵子解凍的存活率、受精率及懷孕率均較慢速冷凍法來得高。因此值得我們介紹給罹癌且未婚的生育年齡婦女,讓她們在接受放射或化學治療前,能以最佳的方式來保留生育能力。 玻璃化冷凍法 快速冷凍法又稱為玻璃化冷凍法,是指藉由快速降低溫度及增加黏稠度的方式將液體物質固體化成為一種「非結晶的玻璃態」。 生物細胞最主要組成分子是水分子,當溫度降低到0℃以下,在一般情況下水分子會形成結晶態的冰晶,而這些冰晶會壓迫細胞內的胞器,進而對細胞造成傷害。在一些特定條件的配合下,細胞在溫度降低的過程中不會形成冰晶,而是變成玻璃化的狀態,其中最重要的三個條件為:溫度的降低速度要快、使用較高劑量的冷凍保護劑,即增加黏稠度、及存放細胞的標本體積要小。當溫度降低到生物標本的「玻璃轉化溫度」(約在零下120℃附近)之下時,標本就不再形成冰晶而達到一個穩定狀態,因此當溫度降低到「玻璃轉化溫度」的速度夠快時,可以儘量減少冰晶的產生。其次,冷凍保護劑可以和細胞內的水分子形成氫鍵,進而避免再溫度下降過程中冰晶的形成。此外,存放細胞的標本體積越小,溫度降低所需要釋放的能量越少,因此能夠越有效率的快速降低標本溫度。玻璃化冷凍法的操作是將生物標本置入含有高濃度冷凍保護劑的培養液中,在幾秒的極短時間內將標本直接置入液態氮筒中,最後降溫至零下150℃以下;置入液態氮後標本的降溫速率高達每分鐘1500℃,若裝置液態氮的容器有抽真空裝置,則其降溫速率可再提高為每分鐘10000℃,如此快的降溫速度可以將冷凍過程對細胞的傷害降至最低,這些傷害包括高濃度冷凍保護劑的細胞毒性、降溫至接近0℃時對胞膜的傷害及上述細胞內冰晶的傷害。解凍過程則將標本置於37℃三秒中,然後將冷凍保護劑的濃度逐漸降低,最後再移入不含冷凍保護劑的培養液中。 現況 Kuleshova等學者於1999年發表第一例玻璃化冷凍人類卵子解凍後成功懷孕的案例,他們使用的冷凍保護劑是40%乙二醇及0.6M蔗糖,而採用的存放卵子標本器材為開放式麥管。玻璃化冷凍人類卵子的第一個大型研究是Yoon等學者於2003年發表,總共冷凍保存了474個卵子,所使用的冷凍保護劑5.5M乙二醇及1.0M蔗糖,而為了增加冷凍速率,他們將卵子標本放在電子顯微鏡所使用的格架上;結果發現冷凍卵子解凍後的存活率為68.7%,解凍後存活卵子受精率為71.7%,每次胚胎植入後懷孕且活產率為21.4%。Chian等人於2005年發表的玻璃化冷凍人類卵子的成功率更高,解凍後的存活率為93.9%,受精率為74.6%,懷孕率則為46.7%,他們使用的冷凍保護劑是乙二醇、丙二醇及蔗糖。Kuwayama等人也於2005年發表的結果也甚佳,解凍後的存活率為90.8%,受精率為89.6%,懷孕率則為41.4%,所使用的冷凍保護劑是乙二醇及蔗糖,而採用的存放卵子標本器材則為開放式的Cryotop。除了上述的器材之外,另外還有一種稱為Cryoloop的器材,將卵子置於一層冷凍培養液薄膜中,好處是液體體積小而接觸表面積大,可將降溫速率最大化。不論是電顯格架、Cryotop、或Cryoloop都屬於開放系統,也就是卵子標本會和液態氮直接接觸,最近有一種密閉系統器材發展出來,稱為Cryotip,應用在卵子冷凍的成果和開放系統一樣好。 安全性 上述玻璃化冷凍卵子的存放器材大多屬於開放系統,標本會直接和液態氮接觸,好處是標本降溫速度快,潛在的風險是液態氮可能散播傳染病。為探討此一可能,有研究將三種牛體病毒污染液態氮後,再將存置於開放式或密閉式器材的玻璃化冷凍牛胚放進上述遭污染之液態氮中,結果發現存置於開放式器材的牛胚有21.3%遭到病毒感染,然而存置於密閉式器材的牛胚則無任何病毒感染。在密閉式玻璃化冷凍卵子器材尚未發展出來之前,因為有上述的微生物感染的風險,使得人工生殖技術專家們裹足不前,不願意嘗試用成功率較高的玻璃化冷凍法來保存卵子,而繼續使用傳統的慢速冷凍法;現在,密閉式玻璃化冷凍卵子器材Cryotip發展出來後,可以避免微生物感染的風險,相信未來會有越來越多人工生殖醫療機構願意採用玻璃化冷凍法來保存卵子,來提高冷凍卵子解凍後的存活率、受精率與懷孕率。 結論 隨著人工生殖技術的進步,冷凍卵子的成功率有大幅的提升,這項技術已從實驗性質邁向臨床應用階段,而玻璃化冷凍卵子法比傳統的慢速冷凍法的成功率更高;密閉式玻璃化冷凍卵子器材已發展出來,其成功率和早期使用的開放式玻璃化冷凍卵子器材一樣好,好處是可以避免微生物感染的風險。現在玻璃化冷凍卵子技術可以應用於罹癌婦女,在接受放射或化學治療前保留其生育能力,協助他們完成孕育下一代的美夢。 名詞中英對照 玻璃化冷凍法 vitrification 甘油 glycerin 葡萄糖 glucosamine 參考資料 1.Kuwayama, M. Highly efficient vitrification for cryopreservation of human oocytes and embryos: the cryotop method. Theriogenology 67, 73-80 (2007). 2.Yavin, S. & Arav, A. Measurement of essential physical properties of vitrification solitions. Theriogeology 67, 81-9 (2007). 3.Jack R. Layne, J., Richard E. Lee, Jr. Adaptations of frogs to survive freezing. Climate Research 5, 53-59 (1995). 4.Kuleshova, L., Gianaroli, L., Magli, C., Ferraretti, A. & Trounson, A. Birth following vitrification of a small number of human oocytes: case report. Hum Reprod 14, 3077-9 (1999). 5.Yoon, T. K. et al. live births after vitrification of oocytes in a stimulated in vitro fertilization-embryo transfer program. Fertil Steril 79, 1323-6 (2003). 6.Chian RC, S. W., Huang JY, Cui SJ, bucket WM, Tan SL. High survival rates and pregnancies of human oocytes following vitrification: pre;iminary report. Fertil Steril 84(Suppl 1), S36 (2005). 7.Kuwayama, M., Vajta, G., Kato, O. & Leibo, S. P. Highly efficient vitrification method for cryopreservation of human oocytes. Reprod Biomed Online 11, 300-8 (2005). 8.Jain, J. K. & Paulson, R. J. Oocyte cryopreservation. Fertil Steril 86 suppl 4, 1037-46 (2006). 9.Bielanski, A., Nadin-Davis, S., Sapp, T. & Lutze- Wallace, C. Viral contamination of embryos cryopresered in liquid nitrogen. Cryobiology 40, 110-6 (2000).
0 評論
陳怡仁 台北榮總婦產部主治醫生
乳癌分兩大類:非侵犯性乳癌和侵犯性乳癌。 非侵犯性乳癌依乳房的組織結構又分為葉狀和乳管兩種。原位癌又稱0期乳癌分成兩類:葉狀原位癌與乳管原位癌。兩者的臨床表現及治療是截然不同易混淆。 葉狀原位癌 指癌細胞在乳腺葉內細胞,屬非侵犯乳癌,不會轉移、癒後良好,治療後幾乎不會復發。目前認為葉狀原位癌並非癌前期病變,轉變為惡性的機率不高,大約每年增加1%,也就是說10年之後只有10%會轉變為惡性腫瘤,因此切片病理診斷後,並不採用手術治療,而是採用觀察性的治療,此外建議病患使用Tamoxifen或是Rolaxifene來降低侵犯性乳癌的發生率,一般建議的使用期限為5年。追蹤的方法:需每年做理學檢查和乳房攝影檢查,若有服用Tamoxifen必須每年做骨盆腔的檢查。 乳管原位癌 乳管原位癌在確定診斷之後,手術治療選擇的原則如下: 一、 手術治療
三、 追蹤
乳癌治療前的診斷 乳癌的診斷,篩檢的方式包括乳房攝影、乳房超音波檢查,若有可能懷疑的病灶,則必須切片。手術前還有一些其他的步驟,包括血液常規檢查、生化檢查、胸部X光檢查,必須時還需要乳房磁振造影,病理切片仍須重新再檢視,評估並換雌激素受體、HER2/neu是否為陽性,此外依不同的期別須追加骨頭掃描、腹部超音波等。 乳房保留手術 乳房保留手術,分成兩種:
不適合乳房保留手術 1. 胸部曾接受放射線治療。 2. 懷疑有惡性乳房腫瘤散佈在整個乳房。 3. 手術前預估乳房保留手術後腫瘤仍無法切除乾淨者。 4. 病患有結締性組織疾病,包括紅斑性狼瘡及硬皮病。 5. 懷孕的婦女。 6. 乳癌大於5公分,在手術前已接受化療,仍無法縮小腫瘤體積。 符合以下5項,乳房保留手術後可不做放射線治療: 1. 病人大於70歲。 2. 腫瘤2公分以下。 3. 腫瘤含有荷爾蒙受體。 4. 無淋巴結轉移。 5. 手術治療後,再接受荷爾蒙治療。 全乳房切除手術 全乳房切除手術,切除範圍為整個乳房,包括乳頭。分成3類:
淋巴根除手術 癌細胞若是已轉移至淋巴結,癌細胞就有較高的機會經血液轉移至其他器官。因此,醫師認為,淋巴結的根除手術會降低乳癌的復發率以及延長病患的存活率。若是要正確的知道腋下淋巴結是否轉移,通常標準的做法會執行腋下淋巴根除手術。另一種狀況是摘取一些少數的淋巴結,這種手術稱哨兵淋巴結採樣,可減少腋下淋巴根除手術的併發症。腋下淋巴根除手術將腋下淋巴結盡可能的清除乾淨,因此副作用比哨兵淋巴結大。不是所有的病患皆需要接受淋巴根除手術,例如0期的乳癌就不需接受淋巴根除手術。 哨兵淋巴結摘除術 所謂哨兵淋巴結是指乳癌轉移時的第一個侵犯的淋巴結,可以利用放射線物質或染劑(Tc-99m labeled sulfur colloid或 methylene blue dye)注射在乳暈或腫瘤附近偵測這些哨兵淋巴結的存在,以同位素接受器探頭或目視藍色染料聚集位置定出。哨兵淋巴結若含有癌細胞,則病患需接受腋下淋巴結根除手術。若哨兵淋巴結是為陰性,則表示其它腋下細胞也為陰性,則不需要接受傳統的腋下淋巴結根除手術。但不完全盡然,意見未真正一致。目前仍認為這兩種摘除術的復發及存活率無顯著差異,唯腋下淋巴結根除手術的併發症較哨兵淋巴結根除手術來的嚴重,副作用一般包括皮膚、手臂的麻木感,肩膀及手臂的活動範圍受限,還會產生水腫的現象。水腫為最常見的副作用,但不至於造成上臂無法活動,併發症的發生率在腋下淋巴結根除手術約佔10%;在哨兵淋巴結採樣約5%。這類合併症影響了生活的品質。 避免水腫的方法: 1. 在接受淋巴結根除手術的手臂,禁止施打靜脈注射的點滴以及量血壓 2. 上臂穿戴彈性繃帶 3. 若有任何不適,應儘速告知醫師 乳房手術方式 絕大部分的乳癌患者都需要接受手術治療,主要手術的有兩大類: 1. 乳房保留手術 2. 全乳房切除手術 乳房保留手術的優點是能保留乳房的外觀,缺點是需接受好幾週的放射線治療。根據過去20年的研究報告顯示,接受乳房保留手術合併放射線治療的存活率與改良式乳房根除手術相同。 乳房手術前,必須考量下列四點: 1. 病患本身對於接受乳房切除後的感受 2. 接受乳房保留手術後,是否有時間接受放射線治療? 3. 於全乳房切除手術後,是否可接受乳房重建手術改善乳房外觀? 4. 若想要盡快減輕心理上的負擔,可選擇全乳房切除手術。 乳房重建手術 乳房重建手術可以在全乳房切除手術時同時做,也可以在乳房手術切除一段時間後再施行。重建的方式包括植入鹽水袋、矽膠及皮瓣轉移。至於採取何種乳房重建方式,根據乳房所需的大小、形狀及病人本身體型、身體狀況,以及有無內科的疾病來決定。 第1期至第3A期的手術治療 侵犯性的乳癌治療較為複雜。對於第一期、第二期及第三期A之手術治療方法有三大類:
第1期至第3A期的輔助治療 對第1期到第3A期術後的輔助治療之決策是根據腫瘤大小以及有無淋巴結轉移來決定。 1. 若腫瘤小於0.5公分或是腫瘤為0.6~1公分但是分化良好:
A. 荷爾蒙受體為陽性,則追加荷爾蒙治療或可考慮接受化學治療。 B. 荷爾蒙受體若為陰性,也可考慮接受化學治療。 3. 若腫瘤大於1公分或是癌細胞轉移至淋巴結大於0.2公分,化學治療則為必要條件。若荷爾蒙受體為陽性,則追加荷爾蒙治療。若HER2/neu為陽性,則追加trastuzumab。 第3期合併局部或淋巴結侵犯的治療 對於第3期合併腫瘤侵犯到胸壁或皮膚、淋巴結的患者,通常會先給予手術前的化學治療,以小紅莓,Doxorubicin,為基礎的化療,此外若腫瘤的HER2/neu有表現,則考慮追加trastuzumab。在術前的化學治療時,若腫瘤已縮小,則可考慮以手術治療。包括全乳房切除或乳房保留手術及淋巴摘除手術,術後再追加化學治療或荷爾蒙治療。若腫瘤並無減少,則考慮追加其他的化學治療甚至是放射線治療,等到腫瘤縮小,再給予手術治療,包括乳房切除或乳房保留手術及淋巴摘除手術。 第4期乳癌的治療 對於第4期的患者,有遠端器官轉移:
B. 若HER2/neu為陰性,則給予化學治療。 名詞中英對照 非侵犯性乳癌 noninvasive breast cancer 侵犯性乳癌 invasive breast cancer 葉狀原位癌 lobular carcinoma in situ, LCIS 乳管原位癌 ductal carcinoma in situ, DCIS 紅斑性狼瘡 systemic lupus erythematosus, SLE 硬皮病 scleroderma 哨兵淋巴結 sentinel lymph node 參考資料
陳怡仁 台北榮總婦產部主治醫生 乳癌分期 癌症的分期是根據腫瘤大小(T)、淋巴轉移的數目(N)及是否轉移(M)至身體其他器官來分期,而分期的重要性是在於可以預知病人預後以及決定治療計劃。 一般癌症的分期是根據TNM來分期: 1. 腫瘤大小 (T分類) 2. 淋巴轉移的數目 (N分類) 3. 遠端轉移 (M分類) T分期: 0期乳癌:如TCIS、LCIS。 T1:腫瘤小於等於2公分。 T2:腫瘤大於2公分,小於等於5公分。 T3:腫瘤大於5公分。 T4:腫瘤已侵犯至胸壁或是皮膚。 N分期: N0:沒有淋巴結轉移。 N1:1~3個淋巴結有癌細胞轉移。 N2:4~9個淋巴結有癌細胞轉移。 N3:大於10個淋巴結有癌細胞轉移。 M分期: M0:遠端器官沒有癌細胞轉移。 M1:遠端器官有癌細胞轉移,例如腦、肝、肺等。 全身性治療
即使在乳癌早期,癌細胞可以透過血液轉移到其他組織,早期轉移時病患並不會有任何症狀,因為早期腫瘤移轉細胞太小,無法藉由一般的影像學檢查或理學檢查發現,因此使用藥物治療癌細胞藉由口服或注射的方式稱為全身性治療。全身性治療根據藥物的不同分成三大類,包括化學治療、荷爾蒙治療、單株抗體治療。荷爾蒙治療通常對荷爾蒙受體陽性的乳癌有效,單株抗體治療只對腫瘤為HER-2陽性的患者有效。舉例來說,若是婦女的荷爾蒙受體為陽性,通常需要接受荷爾蒙治療;若腫瘤為HER-2陽性且大於1公分或合併淋巴結轉移,需要接受單株抗體治療;化學治療根據腫瘤大小、腫瘤分化程度以及有無淋巴結轉移來決定是否使用化學治療。若病患的荷爾蒙受體為陰性、HER-2也為陰性,則全身性治療的方式只能選擇化學治療。 全身性治療執行在手術前後,有不同的名稱,分成輔助性治療及新輔助性治療。輔助性治療就是在手術切除腫瘤後藉由藥物去除無法偵測但已轉移至乳房之外的癌細胞。乳癌患者通常需要接受輔助性治療,除非腫瘤細胞非常小或是分化極為良好才可以不做輔助性治療。若全身性治療執行手術之前稱新輔助治療,此種治療方式是希望於手術前將腫瘤體積減小以便施行乳房保留手術。另外若是病患的乳癌已轉移至全身,全身性治療為最適合的治療方式。 名詞解釋: HER-2/neu:這種抗原是一種腫瘤指標。原來一種基因的受體,可促進細胞生長。若乳癌細胞含有很多HER-2受體,則此癌細胞生長速度較快,在年輕40歲以下的乳癌病患,尤其常見。對於單株抗體,Herceptin的治療有效。 荷爾蒙受體:一種蛋白體位於細胞表面或裡面,能使細胞對血液中循環的荷爾蒙有反應。一般停經婦女,80%乳癌有荷爾蒙受體;年輕的,僅有70%。 放射線治療 放射線治療是使用高能量的射線或粒子去破壞在乳房、胸壁或淋巴結的癌細胞。原則上放射治療的範圍越小越好,因此目前的觀念傾向局部乳房的照射,是乳癌的局部治療工具,通常有兩種主要形式:
放射線治療範圍必須根據下列兩點:
如果接受全乳房切除手術,則放射治療的範圍為整個乳房,在病灶周圍需要補強高劑量的放射線治療,才能降低復發的機會。若接受乳房保留手術,若腫瘤大於5公分或是腫瘤接近切除組織部份的邊緣,在這兩種狀況下,即使接受全乳房切除,也要在傷口周圍皮膚及肌肉組織照射放射線。 此外手術當中,在病灶切除後的空間以及鄰近危險組織,給低能量的放射治療,也是降低復發的局部治療。這種手術中的放療(intraoperative radiotherapy),只用在做過乳房保留手術接受過整個乳房的放療後再有局部復發的病人。雖估有5年以上的歷史,結果不錯,唯病人太少,仍未有結論。 放射線的副作用包括水腫、乳房脹痛,皮膚在日光浴之後的變化,身體虛弱。通常乳房組織及皮膚的變化會持續6~12個月,一部份病人乳房會變的較小、變硬,有的甚至會脹痛。 化學治療 化學治療藥物是指對於癌細胞具有毒性,能消滅癌細胞的藥物。通常經由靜脈注射或是口服使用。乳癌的控制可用單一處方或是混合性處方。根據過去30年臨床研究顯示,化學治療有相當大的療效。目前臨床上使用的原則分成HER2陽性腫瘤、HER-2陰性腫瘤給予不同的處方。通常化學治療會給予幾個治療的週期,輔助性的化學治療需要3~6個月的治療時間。 不同化學治療的藥物有不同的副作用:
噁心、嘔吐。 四肢無力。 味覺的改變。 毛髮的脫落。
血小板數目降低,增加出血、淤青的現象。 紅血素降低,導致身體虛弱。 目前已有良好的藥物可改善噁心、嘔吐,也有良好的藥物可改善紅血球及白血球的降低,可根據狀況來使用。 單株抗體 Trastuzumab(Herceptin),可以對抗HER-2受體陽性的乳癌細胞,可以使用在手術後的輔助治療或是手術前的新輔助治療,也可使用在已轉移的乳癌患者。主要副作用為心臟受損,因此在合併使用其他化學治療時要特別注意,尤其是小紅莓(adriamycin)。 第二種單株抗體Bevacuzumab(Avastin)能抑制血管新生,使用在已轉移的乳癌患者,通常會合併化學治療和紫杉醇Taxol一起使用。能減少腫瘤細胞新生的血管,因為些新生的血管會提供給腫瘤細胞養分及氧氣進而促進乳癌生長,Avastin能減少腫瘤細胞新生的血管,抑制腫瘤生長。 荷爾蒙療法 雌激素大部分由卵巢分泌,此外婦女的脂肪組織及腎上腺也會分泌雌激素。有些乳癌細胞受雌激素作用後,生長速度會變快。目前有許多方法可以降低雌激素的作用。應用在乳癌的治療,有兩種方式:
特別注意這兩種療法對荷爾蒙受體陽性的乳癌患者才有效。於手術之後給予荷爾蒙療法,能降低乳癌的復發率。對已轉移至其他部位而且荷爾蒙受體為陽性的患者也可給予此種治療方式。 荷爾蒙療法只有對乳癌細胞含有雌激素或黃體素受體的患者才會有效,如果患者的腫瘤組織裡沒有雌激素或黃體素受體,就沒有治療效果。 荷爾蒙治療(抗雌激素藥物) 第一種抗雌激素藥物,Tamoxifen是最常使用的抗雌激素藥物。在病患手術之後建議要持續使用5年,可以有效的減少荷爾蒙受體陽性的患者復發的機會,也可使用在轉移性的乳癌患者。但是Tamoxifen會引起更年期不適的症狀,包括燥熱、出汗、陰道乾澀以及情緒上的改變。一般大部分病人都來可接受。 Tamoxifen有兩種較嚴重的副作用: 1. 增加產生子宮內膜癌的機會 2. 增加血栓的機率 第二類可以降低雌激素數量的藥物是芳香酶抑制劑,包括(anastrogole、letrogole、exemestano),可降低更年期婦女雌激素產生之數量,最主要是抑制脂肪組織或是腎上腺所分泌的雌激素,但是無法抑制卵巢所分泌的雌激素數量,因此只適合用在停經後的婦女。 這類藥物比Tamoxifen的副作用少,造成子宮內膜癌和降低血管栓塞的機率很少,但是仍有骨質疏鬆及關節疼痛的副作用。目前,對於更年期乳癌患者荷爾蒙療法首選為芳香酶抑制劑,而非Tamoxifen。 荷爾蒙治療之原則 荷爾蒙治療在以往都是使用Tamoxifen,最近則有芳香酶抑制劑可以降低雌激素的量,特別是在停經後的婦女,因此目前荷爾蒙治療的方式更多元化。也根據停經的前後而有不同。 (1) 更年期婦女:
(2) 對於停經前的婦女在使用Tamoxifen二年至三年之後:
名詞中英對照 單株抗體 monoclonal antibody 荷爾蒙受體 hormone receptor 放射線治療 radiation therapy 小紅莓 adriamycin 紫杉醇 Taxol 芳香酶抑制劑 aromatase inhibitor 參考資料
顏明賢 台北榮民總醫院婦產部婦科主任 婦癌醫學會理事長 子宮頸癌好發於開發中國家,是排名第一的女性癌症死因。而這些國家的醫療資源較為缺乏,無法做到很詳盡的治療前評估及治療。 子宮頸癌的分期,主要以臨床評估為主,而不是其他婦科癌症常用的「手術分期」,最主要的原因是國際婦產科聯盟在1994年所建議的。FIGO堅持子宮頸癌的分期只是為了比較的目的,而不是為了治療的指引。FIGO子宮頸分期的檢查,最主要是婦產科醫師內診的評估,其他包括陰道鏡檢查,子宮頸切片或錐狀手術標本的病理檢查,和簡單的抽血含血液及生化檢查,和胸部X光檢查,除非嚴重案例,如中、晚期病例時,在加上膀胱鏡或直腸鏡的檢查。至於電腦斷層、核磁共振,或甚至腹腔鏡檢查,都不能作分期診斷的依據。 國際間癌症專家,認為子宮頸癌是專指侵襲性子宮頸癌。在台灣民間俗稱「子宮頸原位癌」,並不認為是真正的癌症,目前其名稱較合理應稱為「子宮頸上皮細胞嚴重性病變」,或「子宮頸上皮細胞內贅瘤」,我國健保局也不列入重大癌症疾病。以往我國衛生署公布全國癌症發生的統計圖,子宮頸癌包括原位癌和侵襲癌,而讓國際間醫療專家誤認台灣是子宮頸癌好發的國家。 近年來我國衛生單位與學術和民間團體大力推廣普及婦女子宮頸抹片篩檢,雖然子宮頸上皮細胞內贅瘤明顯增加,但是侵襲性子宮頸癌確實下降許多,這是我國公共衛生的進步。根據2006年衛生署的資料,我國2002年侵襲性子宮頸癌有2107新病例,其年齡標準化為每十萬婦女人口為17.21人,首度低於20人,已經不是女性癌症發生的首位了。 一般對癌症的治療,主要有三種方法:手術、放射治療、及化學治療。手術當然就是開刀拿掉腫瘤,但必須不影響身體生理機能及活動,可能受到腫瘤存在的位置,侵犯範圍,和附近器官侵襲的程度,以及局部淋巴轉移的情形,當然也受到目前身體狀況,包括年齡因素,或其他並存疾病的影響,醫院設備及醫師經驗也要列入考慮。放射治療是以不同輻射熱能,施以局部腫瘤照射,導致腫瘤細胞的死亡。其治療的劑量,除參考標準劑量外,會受到很多因素的影響,如腫瘤體積和侵襲範圍,照射的方法,腫瘤附近正常組織的忍受度,還有病人急性反應的嚴重度。化學治療就是施以化學藥劑,無論是靜脈注射或口服,來抑制腫瘤細胞的生長,甚至凋零死亡。基本上化學治療是針對系統性、全身性,不僅對腫瘤細胞或正常細胞都有毒性,所以有全身性或特殊系統性器官的不良反應或副作用。因此病患本身的身體狀況,併存其他疾病都會影響化學的效果,最主要還是腫瘤細胞本身的生物性,是否會產生抗藥性機轉,及腫瘤體積,會決定化學治療的成敗。 子宮頸癌的治療因此不外乎上述三種方法之ㄧ,或二至三種的綜合療法。因為子宮頸癌常是局部性侵襲的腫瘤,其主要的治療是以手術或放射治療為主。化學治療的地位僅為輔助性療法或緩解性療法。所以一般來說,早期(一、二期)子宮頸癌,是以手術為主;中、晚期(三、四期)子宮頸癌是以放射治療為主,再配合化學治療。對於各分期的治療策略和5年存活率簡述如下(表1、2): 當子宮頸癌首次治療後復發或轉移時,其治療的策略,必須考慮三個條件:
1. 復發或轉移的位置和範圍。 2. 推測復發或轉移的轉機。 3. 首次治療的方法。 如果原先治療是以手術為主,而後復發位置在骨盆中央處,可考慮在手術或放射治療,如果復發位置已侵襲骨盆壁,唯有放射治療。如果原先是以放射性治療為主,而復發位置僅在骨盆中央處,可考慮手術治療,如果以侵襲骨盆壁,需考慮3D的放射治療,如果有遠處轉移,其轉移位置在原先放射治療範圍外,或若有骨頭轉移,產生疼痛症狀,可考慮放射治療。至於已經有多處轉移者,可考慮緩解性化學治療,或支持性治療。 名詞中英對照 國際婦產科聯盟International Federation of Gynecology and Obstetrics, FIGO 陰道鏡檢查 colposcopy 電腦斷層 computed tomography, CT 核磁共振 magnetic resonance imaging, MRI 骨盆 pelvic 趙湘台 醫師
婦癌基金會秘書長 國立陽明大學博士婦產科副教授 台北榮總婦產部婦癌實驗室主任 子宮內膜癌的病因 子宮內膜癌的病因,長期以來均認為導因於不平衡且持續的雌激素刺激所引起。雖說如此,並非所有的子宮內膜癌的病因,均可由無黃體素對抗的雌激素刺激所造成,所以顯然其與其他癌症一樣,仍存有未知的致癌物可導致子宮內膜癌。 子宮內膜癌的危險因子 子宮內膜癌的危險因子,包括肥胖(過重30磅,危險性增為3倍;過重50磅,危險性增為十倍)、低生育狀態(未生育者,增為2倍)、有不正常月經者(過晚停經者(超過52歲)增為2.4倍,停經後常出血者增為4倍)、不排卵者、糖尿病患者(增為2.8倍)、高血壓者(增為1.5倍)、接受內生或外生性長期雌激素刺激而無黃體素對抗者增為9.5倍,另外子宮內膜增生也是一個危險因子,簡單型子宮內膜增生及複雜型子宮內膜增生將來轉變為癌症的比率分別為1%及3%。如果再加上細胞變性或細胞核變性其惡性比例可高達8%及29%。最後,服用乳房癌的預防或輔助荷爾蒙治療病患,也會有2到8倍的危險性,發生子宮內膜癌。 子宮內膜癌好發於停經婦女 因為子宮內膜癌大多發生在50至70歲的婦女,平均年齡為60歲。僅有小於5%的病患年紀小於40歲。約有90%的病患會有不正常的陰道分泌物,80%會有不正常的出血,也有10%的病患抱怨有白帶。其他的症狀多半與腫瘤擴散有關,所以症狀並不專一。 子宮內膜刮搔術的標準的評估工具 最標準的評估子宮不正常出血,就是使用分段性的子宮內膜刮搔或稱擴括術。在子宮頸擴張之前,要先做子宮頸內刮搔術,再做子宮頸擴張及子宮內膜刮搔術。另外抹片檢查也可查探約百分之50之病例。陰道超音波偵測子宮內膜厚度,亦為一種篩檢的工具,不過,診斷還是必須要靠病理切片,所以分段性子宮內膜刮搔術,在任何高危險及高懷疑的病患是必要的。 一旦診斷出為子宮內膜癌,其他的診斷工具,諸如電腦斷層、核磁共振均能協助臨床醫師對此病的治療計劃。 名詞中英對照 子宮內膜癌 endometrial carcinoma 趙湘台博士
台北榮民總醫院婦產部實驗室主任醫師 國立陽明大學婦產科副教授 2002年針對16,608婦女進行5.2年的美國婦女健康關懷研究I和心臟雌激素黃體素補充治療研究兩項臨床試驗,接受雌激素黃體素補充療法的婦女,對於發生乳癌的影響,分別是比起未使用雌激素黃體素補充療法的婦女,其絕對風險每萬人每年分別增加了8(相對風險增加26%,統計上有意義的差異,95%信賴區間介於1.00和1.59之間)和12(相對風險增加27%,但統計上為無意義的差異,95%信賴區間介於0.84和1.94之間)個案例。但在美國婦女健康關懷研究II (WHI II E only) 的 10,739名婦女,進行研究追蹤6.8年後發現,針對接受單獨雌激素治療的婦女,其乳癌發生的風險,每萬人反而減少了7例(相對風險減少26%)。 2003年百萬婦女研究的資料顯示,單獨雌激素治療和雌激素黃體素補充治療的婦女使用者,其增加乳癌的風險分別為1.30 (統計上有意義的差異,95%信賴區間介於1.21和1.40之間) 和2.00 (統計上有意義的差異,95%信賴區間介於1.88和2.12之間)。 迄今,在臨床實驗方面,接受荷爾蒙治療的婦女,統計資料已經累積超過三萬名婦女,而流行病學研究也超過一千八百萬婦女。在其他四項臨床試驗中的12,643名婦女當中,使用單獨雌激素治療,其得到侵犯性乳癌的平均風險是0.81 (統計上無意義的差異,95%信賴區間介於0.63和1.03之間)。在其他四項臨床試驗中的19,756名婦女當中,使用雌激素黃體素合併治療的時候,平均得到乳癌風險是1.24 (統計上有意義的差異,95%信賴區間介於1.03和1.50之間)。 因為臨床試驗的結果,對於黃體素的角色有了較清楚的答案,於是就須探討不同的給與方式會不會影響到乳癌的危險性。所以在雌激素黃體素補充治療中的黃體素用法,就須比較連續性使用黃體素或周期性使用黃體素,對於乳癌發生的風險,有無差異的可能。 在六個流行病學研究當中,包括百萬婦女研究,針對於黃體素的角色做了研究。不管是週期性的或持續性的使用黃體素,其增加乳癌的風險都會增加,二者分別為1.85 (這為統計上有意義的差異,95%信賴區間介於1.72和1.99之間)和1.94 (這為統計上有意義的差異,95%信賴區間介於1.78和2.11之間)。 所以結論是,無論使用那種方式的黃體素治療,都會增加乳癌的風險,而且二種方式的黃體素治療,其間的差異並不顯著。 很有趣的現象顯示,一些流行病學研究,對於使用5年的雌激素黃體素補充治療的停經婦女,發現其所增加的生理風險,並不會比因為具危險因子之生理狀況或生活的改變,所導致的乳癌增加風險高。此些所謂具危險因子之生理狀況或生活的改變包括:生育數少、較少餵母奶、停經年齡延遲10年、更年期肥胖、過度的抽煙和喝酒、以及缺少規律運動的婦女身上。 事實上,接近更年期的婦女的血清中的內生性的性荷爾蒙的濃度上升與增加乳癌的風險更為密切。研究顯示,乳癌風險的增加與血清中內生性的高男性素濃度有關 (統計上有意義的危險性差異倍數(odds ratio:OR)為1.73,95%信賴區間介於1.16和2.57之間);與高androstenedione濃度有關 (統計上有意義的危險性差異倍數為1.56,95%信賴區間介於1.05和2.32之間); 也與高dehydroepiandrosterone sulfate (DHEAS) 濃度有關 (統計上有意義的危險性差異倍數為1.48,95%信賴區間介於1.02和2.14之間)。而和性荷爾蒙結合蛋白的濃度無關。血清中黃體素濃度的升高在統計上則能顯著減少乳癌的風險 (統計上有意義的危險性差異倍數為0.61,95%信賴區間介於0.38和0.98之間)。 對於年紀小於40歲的女人追蹤十年,其得乳癌的風險只在男性素及黃體素的濃度,顯現出來。在男性素濃度較高的前四分之一者,得乳癌的風險為2.6%,而濃度較低的四分之一,得乳癌的風險則為1.5%;而在黃體素濃度較高及濃度較低的四分之一中,罹患乳癌的風險則分別為1.7%及2.6%。相較之下,其他荷爾蒙在血清中的濃度就與乳癌無關。 此外,內生性的性激素濃度在未使用荷爾蒙的停經後婦女也與乳癌有關。研究發現乳癌風險與血中的雌激素和雄性素在統計上有直接的相關性,但並末發現與黃體素或性賀爾蒙結合蛋白有統計上的關連性。當將分析個案限制在有雌激素受體及黃體素受體的乳癌腫瘤病患上並比對其血漿中的荷爾蒙濃度時,發現與高的雌激素濃度 (統計上有意義的危險性差異相對倍數(relative risk:RR)為3.3,95%信賴區間介於2.0和5.4之間);高的androstenedione濃度 (統計上有意義的危險性差異的相對倍數為2.5,95%信賴區間介於1.4和4.3之間) 和高的DHEAS濃度 (統計上有意義的危險性差異相對倍數為2.3,95%信賴區間介於1.3和4.1之間)有正相關,因為其患雌激素受體及黃體素受體的乳癌腫瘤的風險有明顯的上升。此外,所有的荷爾蒙濃度都有與原位病灶強烈相關的傾向,因此,性固醇類荷爾蒙的濃度與有雌激素受體及黃體素受體的乳癌腫瘤是有強烈關係的。 研究停經後使用荷爾蒙的婦女血清中性激素的濃度,結果發現這些婦女與未使用荷爾蒙者相較在統計上有較高的雌激素、游離雌激素、性荷爾蒙結合蛋白、和男性素濃度及較低的游離男性素濃度,在評估荷爾蒙濃度與乳癌風險的關係後,比較濃度較高與較低的各四分之一者下,他們發現游離態雌激素濃度 (這為統計上有意義的危險性差異相對倍數為1.6,95%信賴區間介於1.1和2.7之間)、游離態男性素濃度(這為統計上有意義的危險性差異相對倍數為1.7,95%信賴區間介於1.1和2.4之間)、與乳癌風險有正相關;而性荷爾蒙結合蛋白濃度(這為統計上無意義的危險性差異相對倍數為0.7,95%信賴區間介於0.5和1.1之間),則與乳癌風險不甚相關。 其實以雌激素的濃度對停經後婦女患乳癌的影響更大。因為在60歲以上的婦女其血中雌激素與游離態雌激素的濃度與乳癌的關係更為密切,在統計學上呈現出有意義的危險性差異,其相對危險性倍數分別為2.8 (95%信賴區間介於1.5和5.0之間) 和2.6 (95%信賴區間介於1.4和4.7之間)。 在身高體重指數方面在身體質量指數小於25(公斤/公尺平方)的婦女身上,雌激素的角色對乳癌的影響也有正相關。指數小於25婦女其血中雌激素與游離態雌激素的濃度與乳癌的關係在統計學上呈現出有意義的危險性差異,其相對危險性倍數分別為1.8 (95%信賴區間介於1.1和3.1之間) 和2.4 (95%信賴區間介於1.4和4.0之間)。因此推論,雖然使用荷爾蒙的停經後婦女與不用者的體內荷爾蒙情況可能有所不同,但是血中的荷爾蒙濃度才是決定乳癌的危險因子。 名詞中英對照 美國婦女健康關懷研究I WHI I EP, Women Health Initiative Study 心臟雌激素黃體素補充治療研究 HERS ,Heart and Estrogen/Progestin Replacement Study 百萬婦女研究 MWS ,Million Women Study 男性素 testosterone 性荷爾蒙結合蛋白 sex hormone binding globulin, SHBG 身體質量指數 BMI 參考資料
陳怡仁醫師
台北榮總婦產科主治 乳房是由乳頭、脂肪、乳腺周圍的乳房組織及皮膚所組成。 每個乳房有15~20乳腺葉,每個乳腺葉各有一個乳管通往乳頭。 乳腺的體積會隨著年齡或荷爾蒙而有所變化,例如在青春期時,平坦的胸部會慢慢發育為成熟的乳房。生理期前後,乳房也會明顯的腫脹及消退,而懷孕和哺乳時也會腫脹。乳房的變化和卵巢所分泌出來的雌激又稱動情素及黃體素息息相關。 如要早期發現乳房腫塊,需要每個月自我檢查乳房,並定期追蹤檢查,包括:醫師檢查乳房,乳房超音波、乳房X光攝影檢查,這樣就可以做到早期發現、早期治療了。 乳房自我檢查:
定期請醫師檢查乳房: 20歲以上女性,每 1-2年請醫師檢查一次乳房。 定期接受乳房超音波、乳房X光攝影檢查:
如果發現有乳房良性腫瘤,或是罹患乳癌的高危險群,就需要更密集地定期檢查。 乳房良性瘤的檢查 常見檢查說明
其它可能進行的檢查說明如下:
乳房纖維囊腫 乳房纖維囊腫是一種良性腫瘤,好發於30~50歲的女性,特別是更年期的婦女。女性荷爾蒙在經期、懷孕和哺乳時分泌特別旺盛,當分泌物比較多時,乳腺容易產生一些水泡,學名叫「纖維囊腫」。 水泡小的時候,不會有感覺,如果大到一個程度,又遇上荷爾蒙旺盛的時候,就會出現疼痛的感覺,甚至可以摸到硬塊,女性對於這種忽然生長的腫塊都會非常害怕,以為是乳癌。 纖維囊腫的治療方法有很多種,如果是單一囊腫,醫生多半會採用針刺吸液法,就是利用細針把水抽出來。此外,症狀較明顯的病人還可以服用利尿劑、止痛劑、維他命B、E及月見草,以減輕囊腫所帶來的不適。 纖維囊腫會不會變成乳癌呢?目前並沒有確實的證據顯示纖維囊腫會變成乳癌。 但有統計資料顯示,患有纖維囊腫的女性,得到乳癌的機率比正常人高出2~4倍。因此曾有纖維囊腫的女性一定要加強自我檢查,並且每年到醫院做追蹤檢查。 纖維腺瘤 乳房良性瘤纖維腺瘤是女性最常見的乳房腫塊,而非乳癌。好發於15~35歲。85%的為單一顆,15﹪為多發性(兩顆以上)。 發生原因:乳房纖維腺瘤的發生原因不明,但一般認為與荷爾蒙不平衡有關。 病理組織:纖維腺瘤含有兩種主要組織: 乳腺組織及增生過速的纖維組織。 纖維腺瘤增大情形:纖維腺瘤增大的速度因人而異:有些會變大、有些大小維持不變、有些甚至縮小。一般的纖維腺瘤增大至2~3公分不再增大,且在停經後退化消失。停經後的女性荷爾蒙補充治療會使它增大,懷孕期間或授乳期間亦會增大。 診斷:良性的纖維腺瘤與惡性的乳癌不能單以觸摸感覺來鑑別診斷,醫師仍必須以各種方法區別。常用的方法有乳房X光攝影、乳房超音波、細針抽吸細胞學檢查、切片槍切片檢查、或切除檢查。 一般原則:30歲以下,可以做超音波,細針抽吸細胞學檢查或切片槍切片檢查;30歲以上則建議以超音波或乳房X光攝影、加切片槍切片檢查為佳。 纖維腺瘤與乳癌的關係:大部份的專家認為纖維腺瘤不會轉變為乳癌。但在超音波診斷為良性纖維腺瘤的病灶中,有1~2%為惡性腫瘤,也就是在超音波檢查時有些惡性腫瘤與良性纖維腺瘤一模一樣,因此持續性的追蹤很重要(每3~6個月追蹤)。根據統計,有纖維腺瘤的人,其發生乳癌的比率比一 般人高1.3~1.9倍。若纖維腺瘤內有囊腫、硬化性腺腫大、上皮鈣化、乳突樣變化,則乳癌發生率為一般人的3.1倍。 乳管內乳頭狀瘤 乳管內乳頭狀瘤病常為多發性,可發生於任何年齡的成年女性,但以40~50歲發病者最多見。可分為單發性和多發性兩種。其生物學特性傾向於癌變,癌變率高達30%~40%,可視為癌前病變。 病因:病因尚未確定,但較多的學者認為雌激素過度刺激造成。症狀:多數患者無不適,僅以間歇性、乳頭溢液表現,液體為血性或漿液性。但較大的瘤體若阻塞輸乳管時,可產生疼痛可腫塊,一旦積血排出,腫塊也隨之變小,疼痛緩解。這以現象可反覆出現。 一般而言乳管內乳頭狀瘤的瘤體較小,不容易觸摸到乳腫,輕壓時即可從乳頭溢出血性或咖啡樣液體。 診斷: 乳房X光攝影檢查:乳腺管造影常可顯示腫瘤所在部位及大小,有人報告其診斷符合率可達93.7%。 細胞學檢查:乳頭分泌液塗片,可見紅血球細胞和上皮細胞,偶可找到癌細胞。 超音波檢查:可顯示腫瘤所在部位。 鑒別診斷:
乳房良性瘤的治療
名詞中英對照 正子斷層造影 PET 磁振造影 MRI 乳房纖維囊腫 fibrocyst 乳房良性瘤纖維腺瘤 fibroadenoma 乳管內乳頭狀瘤 intraductal papilloma 參考資料 1.美國衛生院(NIH) 2007 乳癌臨床指引 2.美國國家癌症網(NCCN)乳癌臨床指引 王鵬惠博士 國立陽明大學醫學院婦產科學系副教授
趙湘台博士 台北榮民總醫院婦產實驗室主任醫師 大家都知道並且也接受tamoxifen (一種選擇性雌激素受體調控劑)對乳房癌症的預防及治療上具有顯著的效果。但在國際性乳房癌症評估試驗第一期的研究中,並未顯示出服用tamoxifen對整體乳房癌症的患者任何正面的意義,例如對於這些服用tamoxifen的乳房癌症患者,能夠因治療而得以延長壽命、或改善整體的存活率。問題出在使用tamoxifen的這些乳房癌症的病患,因為tamoxifen的所造成的副作用,例如栓塞的問題,的確奪去很多乳房癌症患者的生命,這些因為藥物所導致的死亡人數,剛好抵消了服用tamoxifen所獲得降低乳房癌症復發的減少病患死亡的效果,也就是說對病患的整體的存活率打了折扣,所以這種挖東牆補西牆的窘況,造成整體乳房癌症病患的存活率,不管有無服用tamoxifen,預後都趨於相似。所以乳房癌症的患者到底要不要服用tamoxifen,就值得我們進一步探討及深思熟慮。最近美國臨床腫瘤學會就提出對於乳房癌症的患者到底要不要服用tamoxifen的利益及壞處做出以下的建議。其重點就是要依據不同族群的病患給與不同的建議。考慮的項目,包括(一)、如果此些婦女服用五年的tamoxifen可以有效的降低乳房癌症的危險性需達到百分之1.66以上,那麼我們才可以建議病患服用五年的tamoxifen;(二)、必須認知tamoxifen仍是一個適當的藥物,在短期之內可以有效的降低乳房癌症的危險性;(三)、危險及利益比必須在使用tamoxifen列入評估,那些婦女可以獲得最大的利益但其相對危險性的卻是最少?例如年輕且是停經前的婦女、這些婦女們幾乎甚少有栓塞的危險性,而且也甚少有子宮內膜癌發生的危險性,或者這些婦女根本已沒有子宮,或是這些婦女具有極高乳房癌症風險的機會,這些婦女可能對於使用tamoxifen的利益危險比值,可得到最大;(四)、目前並無足夠證據顯示服用tamoxifen可以提供婦女有任何增加整體的健康利益或增加整體的存活率的效益。 在我們最近的文章中,我們發現服用tamoxifen而引發的非乳房癌症的不良預後,所以我們清楚的指出對於乳房癌症的預防藥物-tamoxifen,應重新思考。因為新一代的選擇性雌激素受體調控劑 (例如raloxifene)、或是芳香酶的抑制劑(aromatase),或是純雌激素受體對抗劑可能都是較佳的選擇。從2006年四月份,美國醫學公會雜誌刊登出一篇超過兩萬人的跨世紀研究:tamoxifen 和raloxifene的研究 。這個研究發現相對於傳統的tamoxifen在乳房癌症預防的角色,raloxifene這類藥物可能可以提供更多的優點。最主要的根據來自下列兩個觀察;一、tamoxifen與raloxifene這兩種藥物對於乳房癌症的預防,療效毫無軒輊的差別,意謂二者療效平分秋色,二、raloxifene在這個研究中呈現出更少的副作用。這些明顯更少的副作用,甚至也是tamoxifen在乳房癌症預防角色被質疑的部份, 此些所減少的副作用包括了:raloxifene有較少的子宮內膜癌危險性、raloxifene有較少的血液凝固的問題、raloxifene有較少的血液凝固的肺栓塞、raloxifene有較少的白內障。這個raloxifene在預防乳房癌症的療效的發現,並不令人意外,因為raloxifene與tamoxifen都是屬於選擇性雌激素受體調控劑的藥物,所以二者都能在對抗乳房癌症發生,產生降低的效果,也無需大驚小怪。 名詞中英對照 國際性乳房癌症評估試驗第一期 International Breast Cancer Intervention Study I (IBIS-I) trial 美國臨床腫瘤學會 American Society of Clinical Oncology 芳香酶抑制劑 aromatase inhibitor 純雌激素受體對抗劑 pure estrogen receptor antagonist 美國醫學公會雜誌刊 Journal of American Medical Association 參考資料
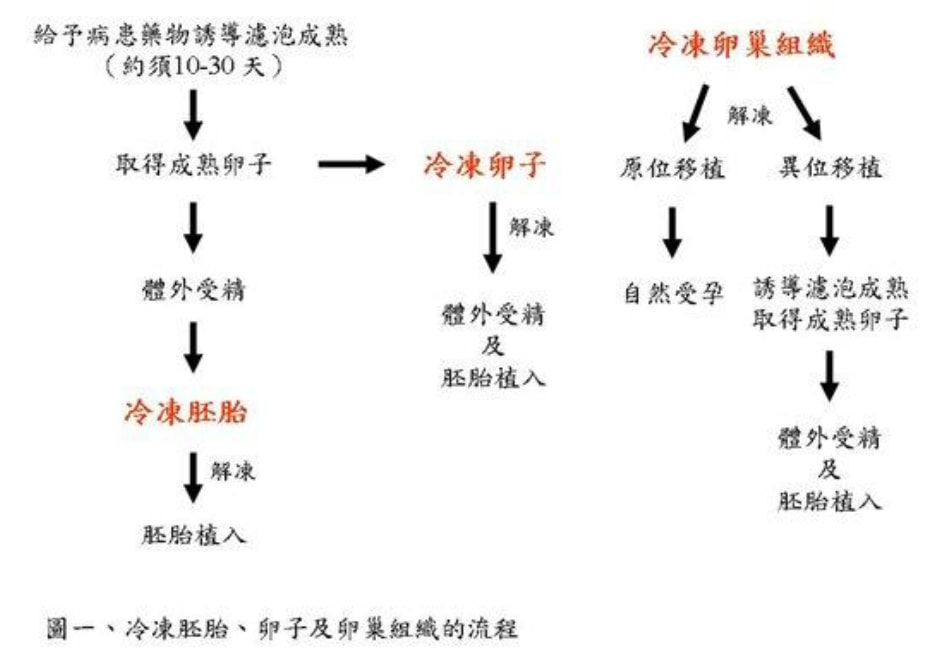
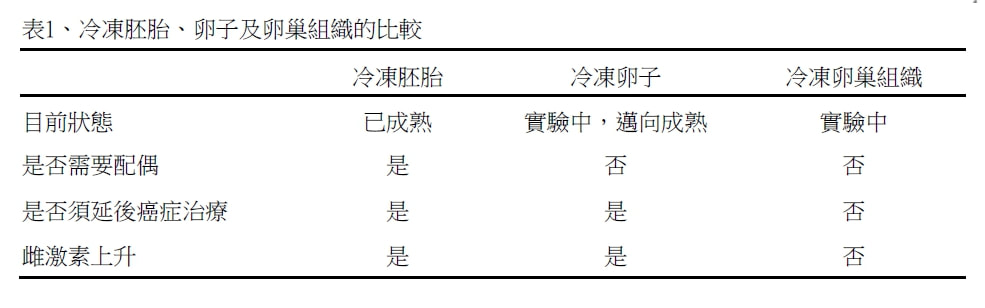
李新揚博士 台北榮總婦產部生殖內分泌科主治醫師 中華民國生育醫學會秘書長 精子和胚胎成功冷凍,早已不是鮮事。由於有了這方面知識和經驗的累積,冷凍卵子,提供生育的另類選擇,已指日可待。 冷凍卵子解凍後成功懷孕的第一例案例在1986年發表,之後的十年內鮮少有成功案例報導。追究其原因,發現冷凍保存會造成卵子外層透明層的硬化,精子受阻,使得受精成功率極低。這種情況到了精蟲細胞內顯微注射技術於1992年發展出來之後才有了改觀。目前冷凍卵子均會配合後續精蟲顯微注射的技術,以提高受精成功率及懷孕率。近年來隨著冷凍卵子的技術的進步,不論是解凍後卵子存活率、受精成功率及懷孕率都有大幅的進步。從2001年約解凍100個卵子才能有一個成功懷孕,進步到現在約解凍10-20個卵子就能有一個成功懷孕。 冷凍卵子在近年來技術上有突破性進展。保存在-196°C的液態氮之下的冷凍卵子,不會有任何的生物反應。細胞在此環境下可以存活幾百年甚至幾千年。唯一的潛在危險是背景輻射每年約0.1 cGy對DNA的傷害。冷凍卵子最危險的時機是發生在冷凍及解凍的兩個過程。最主要造成冷凍傷害的原因在於細胞內冰晶的形成對細胞造成的傷害。為避免冰晶的產生,冷凍的過程須使用冷凍保護劑。冷凍保護劑分為可通透及不可通透兩種:可通透性冷凍保護劑可穿過細胞膜,和水分子形成氫鍵結合以預防冰晶產生,低濃度時可降低結凍溫度,高濃度時可抑制冰晶形成而促進玻璃化,使水分形成像玻璃般的固態而非冰塊;不可通透性冷凍保護劑則只能留在細胞外,使細胞脫水,有助於提高可通透性冷凍保護劑的濃度,及避免解凍過程中滲透壓變化造成的細胞死亡。目前使用的冷凍方式又有慢速冷凍及快速冷凍(也稱為玻璃化)兩種方式。慢速冷凍操作時先在卵子標本加入低濃度冷凍保護劑,然後將標本放入電腦程序冷凍機,以預先設定的程式分階段逐漸降低溫度;快速冷凍則須加入高濃度冷凍保護劑,在幾秒的極短時間內將標本直接置入液態氮中。解凍過程則採取快速解凍,以避免解凍過程中水分的再結晶化對卵子細胞造成的傷害。 隨著環境污染等因素的影響,癌症的發生率有日漸增加的趨勢,美國的統計資料顯示癌症的發生率自1987年至1999年以每年增加0.3%的速度上升;但隨著醫療技術的進步,癌症治療後的存活率逐年提高,自1992年至1999年癌症死亡率每年減少0.6%;其中有8%的女性病患是小於40歲的,她們可能會面臨癌症治療過程中手術、化學治療或是放射治療對於生殖系統造成的不可逆傷害,因此醫界已面臨越來越多罹癌婦女對於保留生育能力的渴求。 癌症治療影響生育能力包括手術,放療和化療三方面: (1) 手術治療:某些婦科癌症有可能必須切除子宮或卵巢,例如子宮頸癌、卵巢癌、及子宮內膜癌。 (2) 放射治療:罹患子宮頸癌、子宮內膜癌、直腸癌或淋巴癌而須要接受腹部及骨盆腔放射治療時,游離輻射會對卵巢造成傷害,進而失去部分或全部的卵巢功能。一般而言,病患年齡越大、照射範圍包含骨盆腔及照射劑量越高,引起卵巢功能的喪失越大。 (3) 化學治療:化療很普遍,影響最廣。許多癌症的治療須要使用單一或多種化學藥物,這些藥物除了對於快速進行有絲分裂的癌細胞會產生毒性外,也可能危及卵子及卵子周圍的顆粒細胞。依照對於卵巢傷害程度,化學藥物可分為高中低三大類:(1) 高傷害性:例如cyclophosphamide、chlorambucil、melphalan、busulfan、nitrogen mustard及procarbazin,(2) 中度傷害:cisplatin、adriamycin,(3) 低度或無傷害性:bleomycin、actinomycin D、vincristine、methotrexate及5-fluorouracil。 罹患癌症的婦女若想保留生育能力,有以下幾種可能的選擇: (1) 保守性手術:早期婦科癌症可考慮只切除病灶,而保留正常的子宮及卵巢組織。例如在病灶2公分以下的子宮頸癌,可考慮子宮頸根除手術(radical trachectomy),保留子宮。 (2) 卵巢移位:為避免放射治療對卵巢的傷害,可考慮在放射治療前動手術將卵巢固定在預定照射範圍之外。 (3)性腺刺激素分泌荷爾蒙類劑:在進行化學治療的同時,這種荷爾蒙類似劑,使卵巢暫時處於休止狀態,以減少化學藥物的毒性,但是其功效目前仍未確定。 (4) 冷凍胚胎:罹癌婦女若有配偶,可考慮採取類似「試管嬰兒」的步驟,即先用給予病患藥物使多個卵巢濾泡成熟,然後在超音波導引下將濾泡中成熟卵子取出,在體外與精子受精,接著將所得到的胚胎予以冷凍保存;待病患癌症痊癒後,再將胚胎解凍並植入其子宮。冷凍胚胎的技術目前已達成熟階段,胚胎解凍後存活率很高。只是此法只能應用在有配偶的病患,而且因為誘導濾泡成熟須要約10到30天,所以癌症治療須因此延後。 (5) 冷凍卵子:對於尚未有配偶的罹癌婦女,冷凍卵子是一個不錯的選擇,此方法也須要給予病患藥物誘導濾泡成熟,再將成熟卵子取出,予以冷凍保存;待病患癌症痊癒且結婚後,再解凍卵子,以先生的精子使其在體外受精,最後將所得到的胚胎植入子宮。卵子的冷凍有其技術上的困難,因為卵子細胞較大且水分較多,使其在冷凍過程中不易脫水,而且成熟卵子的紡綞體也容易受到冷凍傷害;但是最近幾年冷凍卵子技術的進展快速,大幅降低了卵子冷凍過程中的傷害,是單身罹癌婦女保留生育能力不錯的選擇。 (6) 冷凍卵巢組織:若病患的情況須要儘快開始癌症的治療,沒有足夠的時間誘導濾泡成熟,可考慮冷凍卵巢組織,此方法直接以手術方式取得卵巢組織,予以冷凍保存。待病患痊癒後想懷孕時,再解凍卵巢組織,移植到原來卵巢位置(原位移植)或其他部位(異位移植,例如手臂上),原位移植有自然受孕的可能,異位移植則須要靠試管嬰兒技術。目前此項技術仍在實驗階段。僅有零星成功案例報導(冷凍胚胎、卵子及卵巢組織的流程及比較請參考圖一及表1)。 乳癌是目前育齡婦女最常見之癌症,有25%的病人在停經前發病,治療以手術為主,術後若須要化學治療一般在六星期後開始,因此有足夠時間進行冷凍卵子。然而傳統的誘導排卵藥物,FSH,會刺激濾泡分泌雌激素,進而使血清中雌激素大幅上升,有增加乳癌復發風險之疑慮,因此可考慮改用也具有誘導排卵作用的抑制乳癌藥物,tamoxifen及letrozole。Tamoxifen是一種選擇性雌激素受器調節因子,在月經週期第二天或第三天開始使用連續五天,每天40毫克,視濾泡成長情況可酌量增加至每日60毫克。有研究顯示乳癌病患使用tamoxifen比不使用可取得較多之成熟卵子,而在術後追蹤15個月發現使用tamoxifen誘導排卵的乳癌病患復發率並未上升。
Letrozole是第三代芳香酶抑制劑,可以抑制雌激素的生成,是目前新一代治療乳癌的藥物。應用在誘導排卵時,從月經週期第二天或第三天開始使用,每天5毫克,連續使用五天,也可以和低劑量濾泡刺激素FSH合併使用,如此一來FSH刺激卵巢產生的雌激素較低,研究顯示乳癌病患使用letrozole合併FSH日後乳癌復發率也未見升高。子宮內膜癌是另ㄧ個會受到雌激素刺激的癌症,罹患子宮內膜癌婦女若想要冷凍卵子,可考慮使用letrozole,而不用tamoxifen。因為tamoxifen對子宮內膜有刺激作用而有增加子宮內膜癌風險的疑慮。 總之,罹癌婦女保留生育能力方式的選擇,必須考量到病患的病情、治療方式、年齡及婚姻狀態的不同,而有個別差異。冷凍卵子目前仍在實驗階段,但是最近進展快速,若是患者尚無配偶,又有足夠的時間安排誘導排卵的療程時,可以考慮此一方式;若已有配偶則冷凍胚胎是較理想的選擇。因為乳癌及子宮內膜癌會受到雌激素的刺激,所以其誘導排卵藥物的選擇和其他病患不同,乳癌患者可以選擇使用tamoxifen及letrozole,而子宮內膜癌患者則建議使用letrozole。 名詞中英對照 卵子外層透明層 zona pellucida 精蟲細胞內顯微注射 intracytoplasmic sperm injection 冰晶 ice crystal 玻璃化 vitrification 再結晶化 re-crystalization 性腺刺激素分泌荷爾蒙類劑 gonadotropin releasing hormone analog 誘導排卵藥物 follicle stimulating hormone, FSH 參考資料
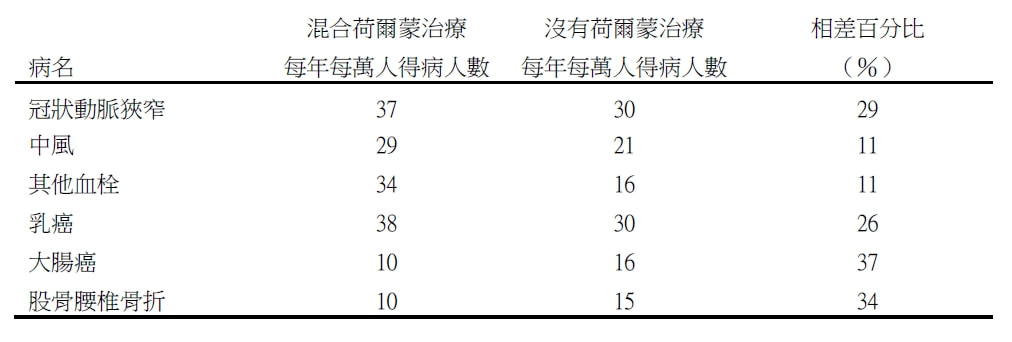
編輯組 針對停經後婦女荷爾蒙治療而言,荷爾蒙一般代表雌激素和黃體素兩種。擁有子宮的停經婦女,通常都合併使用這兩種荷爾蒙。荷爾蒙治療的好壞,由於缺少有規模的大型研究,小作品此起彼落雖未間斷,長久以來,意見仍然分歧。荷爾蒙治療因能改善停經後症候羣,生活品質提升,難免容光煥發,於是婦女趨之若鶩,流行起來。 2002年7月17日,一篇大規模的研究報告,在美國醫學雜誌登出。由於停經後婦女使用荷爾蒙治療的乳癌和心臟病發生率略高於未使用的人,引起一陣騷動。荷爾蒙治療一下子減了一半。在美國,大約有數百萬婦女停止服用荷爾蒙。原來這篇文章,是報導由美國衛生院所支持下的婦女衛生計劃的研究成果。該研究計畫從1991著手,並在1993-1998年間,從美國40個醫學中心,收集16,608名健康停經婦女參與研究,年齡為50-79歲,平均是63歲。其中8,506人接受混合雌激素和黃體素兩種荷爾蒙治療,而8,102人沒有,僅用安慰劑。本來預計在2005年3月完成,時間長達8年5個月。這個研究進行到5.2年,由於發現荷爾蒙治療組的心臟病和乳癌發生率略高於沒有接受荷爾蒙治療的人,同時整體的危險也超過好處。因此提早在2002年5月31日將計劃喊停,並將研究結果刊登出來。主要發現:荷爾蒙治療組得心臟病、中風、其他血栓如肺血栓和乳癌等較多;大腸癌和骨折等則較少。 註: 整體死亡率,荷爾蒙治療和沒有治療人數一樣。大多疾病在研究開始不久便出現,因此短期用荷爾蒙治療未必比較安全。
這個計劃的另一組,針對沒有子宮的停經後婦女,單獨使用雌激素進行研究。發現單獨使用雌激素(CEE)7年後,用雌激素治療的人並沒有增加乳癌的發生率。這個結果,在2004年4月14日,也刊登在美國醫學雜誌上。這個發現,也讓我們連想起來,增加乳癌的原因是否是黃體素?還是雌激素加了黃體素之後才誘發的結果?目前都還沒有答案。 2006年12月14-17日,第29屆聖安東尼乳癌研討會在美國德州召開。研究人員指出,乳癌從1998-2003年開始下降,每年1%。2003年最多下降7%,可能與停用荷爾蒙有關。唯從現有的資料分析,也只能說是推論而已。 台灣的乳癌篩檢率偏低,依健康局去年的報導,僅有8%。與美國比較,顯然我們還停留在美國1998年代之前。近年來台灣的乳癌發生持續的增加,乳癌發生率已高居女性癌症的第一名。我們希望婦女定期檢查乳房;健保局也提供50-69歲婦女,每年一次的免費乳房攝影。請大家提醒大家,一起去做乳癌篩檢,我們的乳癌發生率今後才會減少下來。 名詞中英對照 雌激素 estrogen 黃體素 progestin 美國衛生院 NIH 婦女衛生計劃 WHI, women health initiative study 聖安東尼乳癌研討會 SABC 乳房攝影 mammography 參考資料
熱線追蹤 荷爾蒙治療的新建議... 100309 北美停經協會於2月16日,在分析不同年齡層的停經婦女,用荷爾蒙的好與壞處之後,又有新的建議。接近停經的婦女接受荷爾蒙治療,效果最好;年長或過去未用荷爾蒙的婦女,效果會打折扣。 目前普遍認為,停經婦女使用荷爾蒙,可治療更年期的症狀。婦女衛生計畫研究結果,每天口服合成雌激素0.625mg的劑量,是相當的安全;若再加上黃體素,除少見的中風稍高外,其餘風險都罕見。這次的發現,無論單獨使用雌激素和合併黃體素,風險比婦女衛生計畫所呈現的還要少。不過,不同類別的荷爾蒙,使用方法以及治療時間仍有探討的空間。 荷爾蒙治療領域的17位權威醫師,先回顧了2008年7月所發布每項的建議方針,再納入一些新的證據,共同歸納出這個新的建議。對乳癌、認知能力的降低、癡呆、冠狀心臟疾病與中風的風險,多所著墨。對停用,也有關注,還增列了一些與2008年有不同意見的卵巢癌與肺癌的報導。 荷爾蒙與一般疾病的關係:
荷爾蒙與癌症的關係:
婦女在接受荷爾蒙治療前,應先了解荷爾蒙的利和弊,都應個別考慮。至於,停用的快慢,都不影響臉部潮紅症狀的再現。因此,在停用上,沒有建議。 名詞中英對照 北美停經協會 North American Menopause Society 婦女衛生計畫 Women’s Health Initiative 參考資料 Gass LS M. North American Menopause Society issues guidelines on hormone therapy. Menopause. 2010;17:242-255. |
Copyright © 2018 財團法人中華民國婦癌基金會 All Rights Reserved
會 址:10487臺北市復興北路 178 號 4 樓之 6
聯絡地址:11217臺北市北投區石牌路二段201號中正樓7樓